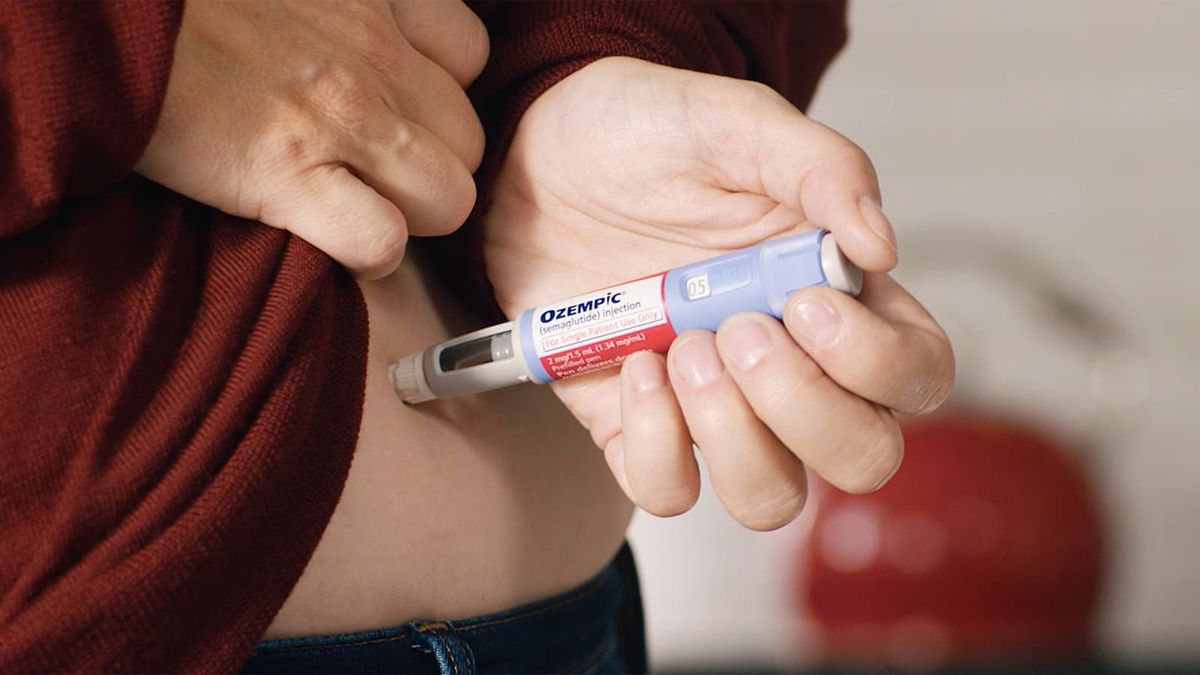
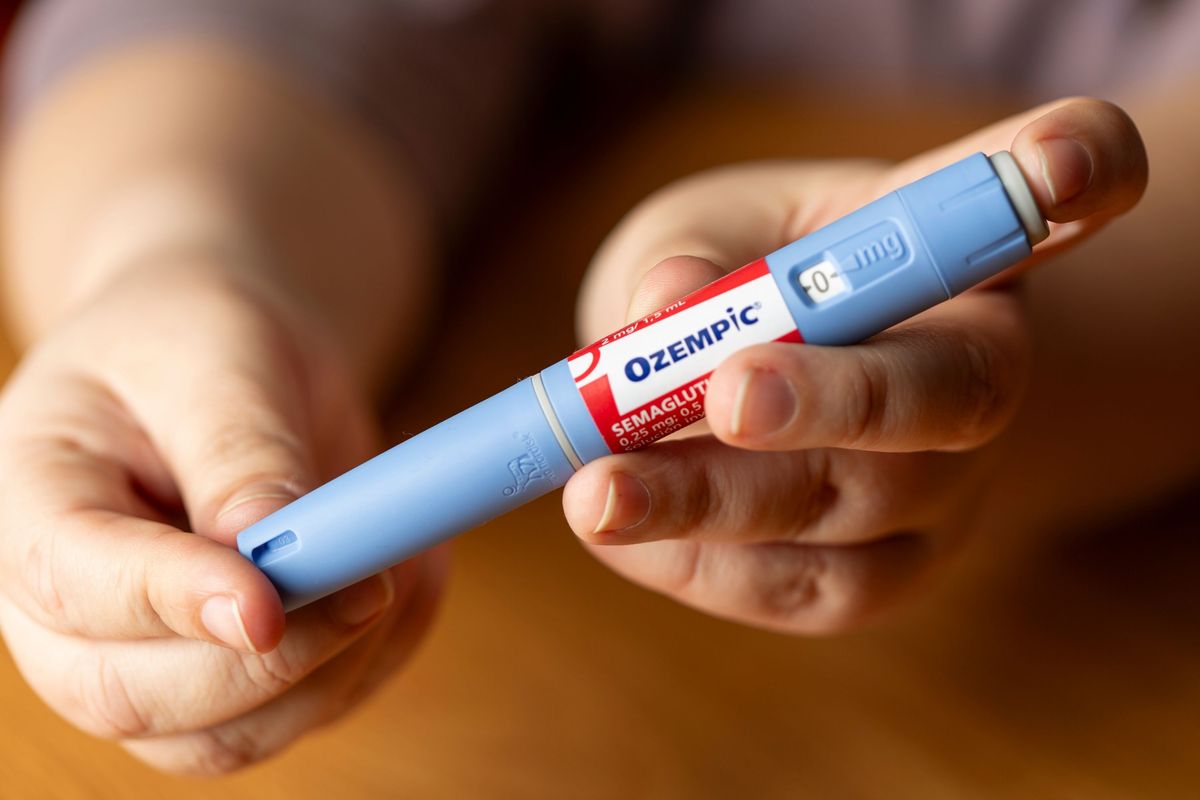
La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) ha lanzado una advertencia muy seria a Novo Nordisk, por no reportar como se debe posibles efectos secundarios de sus fármacos basados en la semaglutida, el principio activo de Ozempic, usado para la diabetes, y para adelgazar .
A NOVO NORDISK
Vea la dura carta de advertencia de la FDA relacionada con Ozempic y efectos secundarios no notificados
La FDA ha lanzado una fuerte advertencia al creador de Ozempic, Novo Nordisk, por posibles efectos secundarios no reportados adecuadamente.
Dura advertencia de la FDA a Novo Nordisk, creador de Ozempic
La FDA envió una carta de advertencia a Novo Nordisk, el pasado 5 de marzo de 2026, en la que le informa algunas faltas en cuanto al reporte de posibles efectos secundarios en personas que usaron semaglutida.
Ozempic y Wegovy, ambos de Novo Nordisk, contienen semaglutida que pertenece a una clase de medicamentos conocidos como agonistas de los receptores del péptido-1 similar al glucagón (GLP-1).
"Esta Carta de Advertencia le informa sobre las condiciones objetables observadas durante la inspección de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) realizada en su empresa, Novo Nordisk Inc. (en adelante, NNI), entre el 13 de enero y el 7 de febrero de 2025", comienza la misiva.
De acuerdo con la FDA, los funcionarios revisaron el cumplimiento de la empresa respecto a las regulaciones sobre experiencias adversas a medicamentos posteriores a la comercialización (PADE).
Esto supone inspecciones y programas de cumplimiento de la FDA para monitorear los efectos secundarios de los fármacos cuando ya están en el mercado.
"La inspección reveló graves infracciones a los requisitos de notificación de PADE". apuntó la FDA.
Fallecimientos de pacientes que tomaron semaglutida, el principio activo de Ozempic
Algunos ejemplos de fallas incluyen que "la empresa no notificó los eventos adversos graves e inesperados a la FDA en un plazo de 15 días naturales, como lo exigen las regulaciones de PADE".
En la carta también se hace referencia a tres fallecimientos de pacientes que tomaban semaglutida y que supuestamente no se informó de forma adecuada a la agencia.
"Por ejemplo, el caso Argus n.° 1171264 incluye a una persona no profesional de la salud que reportó el fallecimiento de un paciente que recibía semaglutida; sin embargo, usted no investigó con prontitud porque no se obtuvo el consentimiento del informante y este no era profesional de la salud, como se indica en su procedimiento escrito. Este caso se cerró sin que usted lo reportara a la FDA", precisa.
Entre los casos se incluye uno en el que un médico informó al representante de la empresa que un paciente que tomaba semaglutida estaba deprimido y se suicidó.
Novo Nordisk no tardó en responder.
"Novo Nordisk se toma muy en serio los requisitos de notificación de PADE y planeamos abordar las solicitudes de la Carta de Advertencia de manera rápida e integral", afirmó Anna Windle, jefa de desarrollo clínico, asuntos médicos y regulatorios de Novo Nordisk US, recoge CBS News.
"Estamos seguros de que resolveremos los asuntos descritos en la Carta de Advertencia a plena satisfacción de la FDA", agregó.
Carta de advertencia de la FDA a Novo Nordisk
Sr. David S. Moore N.º de referencia de la FDA: 26-HFD-45-03-01
Presidente
Novo Nordisk Inc.
800 Scudders Mill Road
Plainsboro, Nueva Jersey 08536
Estimado señor Moore:
Esta Carta de Advertencia le informa sobre las condiciones objetables observadas durante la inspección de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) realizada en su empresa, Novo Nordisk Inc. (en adelante, NNI), entre el 13 de enero y el 7 de febrero de 2025. Los investigadores que representan a la FDA revisaron su cumplimiento con las regulaciones sobre experiencias adversas a medicamentos posteriores a la comercialización (PADE). La inspección reveló graves infracciones a los requisitos de notificación de PADE que se encuentran en la sección 505(k) de la Ley Federal de Alimentos, Medicamentos y Cosméticos (Ley FD&C) [21 USC 355(k)] y el Título 21 del Código de Regulaciones Federales (21 CFR) 314.80. El incumplimiento de la sección 505(k) es un acto prohibido según la sección 301(e) de la Ley FD&C [21 USC 331(e)].
Esta inspección se llevó a cabo como parte del Programa de Monitoreo de Bioinvestigación de la FDA, que incluye inspecciones diseñadas para garantizar que se envíen datos de seguridad precisos, confiables y oportunos a la FDA para el monitoreo de la seguridad del producto y para garantizar el cumplimiento de las regulaciones PADE.
Al finalizar la inspección, los investigadores le presentaron y analizaron el Formulario FDA 483, Observaciones de la Inspección. Acusamos recibo de su respuesta por escrito al Formulario FDA 483, con fecha del 3 de marzo de 2025, y de su correspondencia posterior con fechas del 11 de abril de 2025, 2 de mayo de 2025, 6 de junio de 2025, 11 de julio de 2025, 19 de septiembre de 2025, 31 de octubre de 2025 y 15 de enero de 2026.
De nuestra revisión del Informe de Inspección de Establecimientos de la FDA, los documentos presentados con ese informe y su respuesta escrita y correspondencia con fechas 3 de marzo de 2025, 11 de abril de 2025, 2 de mayo de 2025, 6 de junio de 2025, 11 de julio de 2025, 19 de septiembre de 2025, 31 de octubre de 2025 y 15 de enero de 2026, parece que usted no cumplió con los requisitos legales aplicables de la Ley FD&C y las regulaciones aplicables contenidas en 21 CFR parte 314.
Deseamos destacar lo siguiente:
No desarrollar procedimientos escritos para la vigilancia, recepción, evaluación y reporte de experiencias adversas a medicamentos posteriores a la comercialización (EAM) a la FDA como lo exige 21 CFR 314.80(b).
Como titular de solicitudes de productos con principios activos como semaglutida, liraglutida, nedosiran sódico y estradiol, NNI debe desarrollar procedimientos escritos para la vigilancia, recepción, evaluación y notificación de experiencias adversas a medicamentos (EAM) poscomercialización a la FDA. Usted desarrolló procedimientos escritos que no garantizaron que usted y su contratista, que actúa en su nombre, cumplieran con todas las regulaciones aplicables de EAM para la vigilancia, recepción, evaluación y notificación de EAM.
Algunos ejemplos de esta falla incluyen, entre otros, los siguientes:
1. No desarrolló procedimientos escritos, según lo exige el Título 21 del Código de Regulaciones Federales (CFR), 314.80(b), que garantizaran que usted y su contratista, actuando en su nombre, informaran a la FDA sobre todos los ADE graves e inesperados en un plazo de 15 días naturales, de conformidad con el Título 21 del CFR, 314.80(c)(1)(i). La normativa sobre ADE exige que el solicitante informe sobre cada ADE grave e inesperado, ya sea nacional o internacional, en un plazo máximo de 15 días naturales a partir de la recepción inicial de la información (Título 21 del CFR, 314.80(c)(1)(i)). En concreto:
a. Su procedimiento escrito Q014048, “Manejo de Eventos Adversos y Otra Información de Seguridad” (Versión: 28.0, Fecha de Vigencia: 03 Oct 2024), permitía que los ADE reportados al NNI fueran rechazados o cancelados (y, por lo tanto, no reportados a la FDA) si el reportador consideraba que el ADE no estaba relacionado con el producto. Específicamente, el procedimiento Q014048 excluye los reportes de la definición de “reacción adversa” si “los reportadores declaran específicamente que creen que los eventos no están relacionados o que se puede excluir una relación causal”. Esta definición es incompatible con las regulaciones de la FDA, que definen un ADE como “cualquier evento adverso asociado con el uso de un medicamento en humanos, ya sea que se considere relacionado con el medicamento o no”. Las regulaciones de la FDA requieren que los solicitantes desarrollen procedimientos escritos para, entre otras cosas, el reporte de ADE, independientemente de si el evento se considera causalmente relacionado con el producto. Un ADE que se determine como grave e inesperado debe reportarse a la FDA a más tardar 15 días después de la fecha de recepción inicial. Con base en su procedimiento escrito, su personal o contratista canceló o rechazó eventos adversos graves e inesperados que debían notificarse en un plazo de 15 días naturales, ya que documentaron que estos eventos no estaban relacionados con el producto. Por ejemplo, el caso Argus 1 n.° 1331385 involucra a un consumidor que quedó discapacitado tras sufrir un derrame cerebral, que constituye un evento adversos graves e inesperados, mientras recibía liraglutida. El consumidor informó que el derrame cerebral no estaba relacionado con la liraglutida; por lo tanto, usted rechazó este caso. En consecuencia, no notificó los eventos adversos graves e inesperados a la FDA en un plazo de 15 días naturales, como lo exigen las regulaciones de PADE.
Durante la inspección, usted declaró que abrió la desviación DV0166369 en abril de 2024 tras descubrir que no todos los ADE graves e inesperados notificables se habían presentado a la FDA, ya que su personal o contratista los había cancelado o rechazado y se habían documentado como "incidentales" o "incidentales y no relacionados". Identificó sus procedimientos escritos, incluido el Q014048 (tanto la versión actual como las anteriores), como la causa raíz de esta desviación, ya que tanto la versión actual como las anteriores permitían que los ADE notificados a NNI se rechazaran o cancelaran basándose en la evaluación del notificador de la falta de causalidad del evento con el producto. El análisis de la causa raíz indicó que, si bien la exclusión de ciertos ADE de la notificación, como se describe en los procedimientos escritos, era coherente con las regulaciones de las autoridades reguladoras extranjeras, no lo era con las regulaciones estadounidenses. Si bien cerró la desviación DV0166369 en diciembre de 2024, no se aseguró de que sus medidas correctivas y preventivas se implementaran eficazmente para resolver los problemas existentes y evitar la recurrencia del incumplimiento. Específicamente, si bien se aseguró de que las versiones anteriores de Q014048 ya no estuvieran en uso, no actualizó la definición de "reacciones adversas" para eliminar las referencias a la relación y causalidad en la versión actual de Q014048. Además, cerró la desviación DV0166369 sin confirmar la finalización de su acción correctiva para enviar todos los ADE graves e inesperados reportables a la FDA. Si bien declaró en su respuesta escrita que envió estos ADE a la FDA después de que los investigadores los analizaran con usted durante esta inspección, no proporcionó los números de caso ni las fechas de envío a la FDA para todos los casos con ADE graves e inesperados que se identificaron como parte de la desviación DV0166369. Como resultado, la FDA no puede verificar que todos los ADE graves e inesperados identificados en esta desviación se enviaran a la FDA. Además, no proporcionó suficiente información sobre cómo implementará las acciones correctivas y preventivas identificadas en esta desviación para garantizar que todos los ADE graves e inesperados se notifiquen a la FDA.
En su respuesta escrita del 3 de marzo de 2025 y en correspondencia posterior, describió medidas correctivas, entre ellas: (1) la revisión de los procedimientos y otros documentos para eliminar terminología que generaba ambigüedad y que provocaba que no se informara a la FDA de eventos adversos graves e inesperados (ADE); (2) la actualización de las definiciones y la documentación del término "casos espontáneos"; y (3) la realización de una revisión retrospectiva de los casos para garantizar que todos los casos válidos se presentaran a la FDA. Además, indicó que todos los casos identificados como informes de alerta de 15 días, como parte de la desviación DV0166369, se habían presentado a la FDA al 6 de febrero de 2025.
Si bien reconocemos las medidas correctivas y preventivas que ha tomado o planea tomar, su respuesta escrita y la correspondencia posterior son insuficientes porque no proporcionó suficientes detalles para que la Agencia determine si sus acciones resolvieron eficazmente los problemas existentes y evitarán infracciones similares en el futuro. En concreto, no proporcionó suficientes detalles sobre cómo sus procedimientos, directrices y materiales de capacitación actualizados garantizarán el cumplimiento futuro de la notificación oportuna de ADE graves e inesperados a la FDA.
b. Su procedimiento escrito Q014048, “Manejo de Eventos Adversos y Otra Información de Seguridad” (Versión: 28.0, Fecha de Vigencia: 3 de octubre de 2024), establece que los criterios mínimos para que los Informes de Seguridad de Casos Individuales (ICSR) se presenten de forma expedita son: (1) uno o más informantes identificables; (2) un solo paciente identificable; (3) un producto NNI sospechoso; y (4) una reacción adversa sospechada. Sin embargo, su procedimiento escrito no garantizó que usted y los contratistas del centro de llamadas que actuaron en su nombre recibieran, revisaran y procesaran correctamente la información sobre ADE, lo que resultó en la imposibilidad de presentar los ADE graves e inesperados que debían notificarse a la FDA en un plazo de 15 días naturales.
Específicamente, usted y sus contratistas invalidaron indebidamente los informes de alerta de 15 días debido a la falta de identificadores de pacientes; sin embargo, durante la inspección, la FDA identificó identificadores de pacientes válidos en los documentos fuente de estos informes. Estos informes no se presentaron a la FDA hasta que se analizaron con usted durante la inspección. Por ejemplo, el caso Argus n.° 1342548 incluye a un consumidor que informa el fallecimiento de un paciente masculino que recibió semaglutida; sin embargo, usted invalidó el caso porque no registró el identificador del paciente. Durante la inspección, la FDA encontró el identificador del paciente en los documentos fuente de este caso. Como resultado de esta invalidación errónea, usted no reportó eventos adversos graves e inesperados a la FDA dentro de los 15 días calendario, como se requiere.
Notamos que usted identificó este problema cuando (b)(4) actuó como su contratista del centro de llamadas entre el 12 de mayo y el 12 de octubre de 2023. Posteriormente, usted rescindió su contrato con (b)(4) y cambió a su contratista del centro de llamadas a (b)(4) , a partir del 13 de octubre de 2023. También abrió la desviación DV0155511 en diciembre de 2023 en respuesta a los problemas observados con (b)(4) . Aunque cambió a su contratista del centro de llamadas a (b)(4) y completó las acciones correctivas y preventivas como parte de la desviación DV0155511, continuó invalidando los casos de ADE por falta de un identificador de paciente, a pesar de que los identificadores de paciente estaban disponibles de acuerdo con el procedimiento escrito Q014048 y los casos, de otro modo, calificaban como reportables. Por lo tanto, no se aseguró de que sus acciones correctivas y preventivas (por ejemplo, revisión y creación de recursos de capacitación y contenido para proveedores) se implementaran de manera efectiva para resolver los problemas existentes y evitar la recurrencia del incumplimiento.
En su respuesta escrita del 3 de marzo de 2025 y en correspondencia posterior, usted indicó las acciones correctivas propuestas, incluyendo, entre otras: (1) realizar revisiones retrospectivas de casos para garantizar que todos los casos válidos se enviaran a la FDA; (2) redactar instrucciones de trabajo relacionadas con los controles de calidad y verificación de ICSR, incluida la verificación de datos de origen; (3) planificar un enfoque gradual para la transición de la admisión de casos de seguridad de los agentes del centro de llamadas contratados a agentes de seguridad del paciente internos dedicados, que son profesionales de la salud; (4) realizar una evaluación del programa de gestión de proveedores; y (5) crear un equipo de gestión de proveedores, un equipo de calidad de proveedores y un equipo de capacitación dedicado a su equipo de seguridad del paciente de EE. UU., para garantizar la capacitación y supervisión adecuadas de los proveedores.
Si bien reconocemos las medidas correctivas y preventivas que ha tomado o planea tomar, su respuesta por escrito es insuficiente porque no proporcionó información sobre si las medidas propuestas evitarán infracciones similares en el futuro. Por ejemplo, no proporcionó información específica sobre cómo garantizará que los proveedores que actúen en su nombre reciban, revisen y procesen correctamente la información de ADE, ni cómo mantendrá la supervisión relacionada con las funciones delegadas. En concreto, no proporcionó suficientes detalles sobre cómo operarán sus equipos de Gestión de Proveedores, Calidad y Capacitación, cuáles serán sus actividades ni cómo estos equipos garantizarán que los contratistas que actúen en su nombre capturen de forma precisa y completa los ADE, realicen actividades de control de calidad y cumplan con todos los requisitos PADE aplicables. Además, no describió cómo operará el centro de llamadas "interno" ni proporcionó información adecuada para garantizar que su centro de llamadas interno cumpla con los requisitos PADE en el futuro.
c. Su procedimiento escrito Q040018, “Manejo de Casos Individuales de Seguridad en la Base de Datos Global de Seguridad” (Versión 43.0, Fecha de Vigencia: 17 de mayo de 2024), establece que la mayoría de las reacciones adversas graves deben ingresar a revisión médica antes del noveno día calendario posterior a la fecha de conocimiento y completar la revisión médica antes del décimo día calendario posterior a dicha fecha. Sin embargo, su procedimiento escrito no garantizó que los casos completaran la “revisión médica” dentro de los plazos especificados. Por el contrario, los casos permanecieron en estado de “revisión médica” más tiempo del especificado en su procedimiento escrito, lo que resultó en que usted no presentara los informes de alerta de 15 días a la FDA dentro del plazo requerido. Durante la inspección, la FDA identificó y le informó sobre ADE graves e inesperados que no se presentaron a la FDA porque permanecieron en estado de “revisión médica” más allá del plazo especificado en sus procedimientos escritos. Por ejemplo, en el caso Argus n.° 1334278, usted recibió información el 9 de diciembre de 2024 de un consumidor que reportó ideación suicida mientras tomaba semaglutida. Este caso entró en estado de "revisión médica" el 16 de diciembre de 2024; sin embargo, la revisión médica no se realizó hasta el 3 de febrero de 2025, después de ser identificado durante la inspección de la FDA, y el caso se presentó a la FDA el 5 de febrero de 2025. Como resultado, no informó ADE graves e inesperados a la FDA dentro de los 15 días calendario, como lo exigen las regulaciones PADE.
En su respuesta escrita del 3 de marzo de 2025 y en su correspondencia del 11 de abril de 2025, usted indicó que sus medidas correctivas incluían, entre otras, la exigencia de una revisión diaria de los casos de seguridad del paciente en cada estado del flujo de trabajo. Sin embargo, su respuesta escrita es insuficiente, ya que no proporcionó información sobre si las medidas propuestas evitarán infracciones similares en el futuro. Por ejemplo, no proporcionó suficientes detalles sobre la causa raíz de esta infracción, ni por qué estos casos permanecieron en estado de "revisión médica" más allá de los plazos especificados en su procedimiento escrito. Tampoco ha evaluado si este problema afecta, y en qué medida, la notificación oportuna de otros casos de su cartera de productos.
2. No desarrolló procedimientos escritos que garantizaran la pronta investigación de todos los ADE sujetos a informes de alerta de 15 días, de conformidad con el Título 21 del Código de Regulaciones Federales (CFR), Sección 314.80(c)(1)(ii). Las regulaciones de PADE exigen que el solicitante investigue con prontitud todos los ADE sujetos a informes de alerta de 15 días posteriores a la comercialización (CFR, Sección 314.80(c)(1)(ii)).
Su procedimiento escrito Q0360683, “Flujo de trabajo de gestión de casos en Novo Nordisk Inc. Seguridad del paciente” (Versión: 7.0, Fecha de aprobación: 4 de noviembre de 2024), establecía que no se requería seguimiento de los ADE notificados si no se obtenía el consentimiento del notificador y si este no era un profesional de la salud. Con base en este procedimiento escrito, usted y su contratista, actuando en su nombre, no investigaron con prontitud los ADE sujetos a la notificación de alertas de 15 días, ya que no se comunicó con los notificadores para solicitar información adicional a menos que se obtuviera explícitamente el consentimiento del notificador. Las regulaciones PADE no exigen la obtención del consentimiento para obtener información adicional. En consecuencia, no investigó los ADE graves e inesperados según lo exigen las regulaciones PADE.
Por ejemplo, el caso Argus n.° 1171264 incluye a una persona no profesional de la salud que reportó el fallecimiento de un paciente que recibía semaglutida; sin embargo, usted no investigó con prontitud porque no se obtuvo el consentimiento del informante y este no era profesional de la salud, como se indica en su procedimiento escrito. Este caso se cerró sin que usted lo reportara a la FDA.
El procedimiento Q0360683 también requería que NNI realizara dos intentos de seguimiento en casos graves con reporte de fallecimiento, a fin de obtener información de seguridad relevante para su reporte a la FDA. Sin embargo, usted no investigó con prontitud el caso Argus n.° 1079792, en el que un médico informó a su representante de la empresa que un paciente que tomaba semaglutida estaba deprimido y se suicidó. Usted no documentó ningún intento de obtener información adicional del reportador, incluyendo los identificadores del paciente. A la fecha de emisión de esta carta, este caso no se ha presentado a la FDA.
En su respuesta escrita del 3 de marzo de 2025, usted atribuyó la falta de investigación oportuna de los ADE graves e inesperados a una laguna procesal que requería el consentimiento innecesario del denunciante. En su respuesta escrita y en la correspondencia posterior, usted describió las acciones correctivas, incluyendo, entre otras: (1) revisar los procedimientos operativos estándar (POE) y las capacitaciones locales y globales para eliminar el requisito de obtener el consentimiento de los denunciantes para el seguimiento; (2) eliminar los campos que requieren el consentimiento de los denunciantes de las plataformas de TI locales; (3) enviar una comunicación a todos los proveedores y revisar las plantillas del acuerdo de intercambio de datos de seguridad operacional (SDEA) para aclarar que el consentimiento no es un requisito predicado para la recopilación de información de un denunciante; y (4) realizar una revisión retrospectiva de los casos para evaluar que se realizaron intentos de seguimiento con los denunciantes en el momento y la documentación adecuados. Sin embargo, su respuesta escrita es inadecuada porque no proporcionó información sobre cómo sus acciones correctivas propuestas o completadas evitarían infracciones similares en el futuro. Por ejemplo, no proporcionó detalles suficientes sobre sus actividades de control de calidad, incluido cómo mantendrá la supervisión de los proveedores con los que contrata para cumplir con cualquiera de sus responsabilidades de ADE.
Además, su respuesta escrita no abordó específicamente cómo realizará el seguimiento adecuado, como lo exige 21 CFR 314.80(c)(1)(ii), para los informes de alerta de 15 días que no se presentaron al momento de la inspección.
En su respuesta escrita del 3 de marzo de 2025, y en correspondencia posterior, describió las medidas correctivas, incluyendo, entre otras, la contratación de un consultor para la revisión de sus procesos de farmacovigilancia e interfaces asociadas, así como de su sistema de desviaciones y su sistema de acciones correctivas y preventivas, a fin de garantizar que todos los casos se hayan notificado a la FDA y que todas las desviaciones se hayan gestionado adecuadamente. También indicó que su consultor está realizando una revisión retrospectiva de todas las desviaciones cerradas relacionadas con la farmacovigilancia desde junio de 2017, y que ha creado un comité de revisión de desviaciones. Reconocemos que su revisión retrospectiva de las desviaciones ha finalizado y que ha recibido el informe final. Para cada desviación importante que pueda afectar el cumplimiento de las regulaciones PADE y que tenga una fecha de aprobación de Garantía de Calidad posterior al 1 de enero de 2021, incluidas las enumeradas en la solicitud de Manejo de Desviaciones proporcionada a los investigadores durante la inspección, debe enviar una descripción de la desviación, la fecha de identificación, el estado actual, el análisis de causa raíz, una evaluación del impacto, el estado de todas las acciones correctivas y preventivas, y el cronograma y los resultados de los controles de efectividad.
Si bien reconocemos las medidas correctivas y preventivas que su empresa ha implementado desde nuestra inspección, su respuesta es insuficiente debido a que no proporcionó suficientes detalles para determinar si sus acciones evitarán eficazmente infracciones similares en el futuro. Sus explicaciones, al considerar las infracciones descritas anteriormente y su incapacidad para abordar adecuadamente su incumplimiento, sugieren fallas sistémicas en la vigilancia, recepción, evaluación y notificación de ADE a la FDA. Además, su incapacidad para identificar y evaluar la(s) causa(s) raíz de las deficiencias mencionadas en esta carta genera inquietud sobre la capacidad de su empresa para monitorear la seguridad de sus productos, incluyendo la supervisión de los proveedores con los que contrata para cumplir con sus responsabilidades en materia de ADE. Si bien esta inspección se centró en el cumplimiento por parte de NNI de las regulaciones PADE para una muestra de sus productos, incluyendo semaglutida, liraglutida, nedosirán sódico y estradiol, con base en la naturaleza de los hallazgos de la inspección y su respuesta escrita y correspondencia, tenemos serias preocupaciones sobre el alcance y el impacto de estas infracciones en toda su cartera de productos.
La FDA depende de la presentación completa, precisa y oportuna de los ADE para supervisar el perfil de seguridad de un producto y cumplir con su misión de proteger y promover la salud pública. Informar a la FDA sobre los ADE dentro de los plazos establecidos es necesario para el seguimiento continuo de los perfiles de seguridad de los medicamentos. No informar ni investigar los ADE puede limitar la información de seguridad que la FDA necesita para supervisar posibles señales de seguridad.
Enfatizamos que, como titular de una solicitud, es su responsabilidad asegurarse de cumplir con todos los requisitos PADE aplicables, incluso al contratar a un proveedor para que cumpla con cualquiera de sus responsabilidades ADE. Su falta de desarrollo de procedimientos que garanticen la presentación de informes de alerta de 15 días y la pronta investigación de los ADE que fueron objeto de dichos informes genera serias dudas sobre su capacidad para reportar de forma precisa y completa la información sobre la seguridad del producto a la FDA, de acuerdo con los requisitos PADE.
Esta carta no pretende ser una lista exhaustiva de las deficiencias existentes en NNI. Es su responsabilidad garantizar el cumplimiento de todos los requisitos legales y las regulaciones pertinentes de la FDA. Debe abordar cualquier deficiencia y establecer procedimientos para garantizar el cumplimiento de las regulaciones de la FDA.
Si está considerando tomar alguna medida que probablemente provoque una interrupción en el suministro de medicamentos producidos en sus instalaciones, la FDA le solicita que se comunique de inmediato con el Equipo de Escasez de Medicamentos del CDER a [email protected] para que la FDA pueda colaborar con usted en la manera más eficaz de que sus operaciones cumplan con la ley. Contactar al Equipo de Escasez de Medicamentos también le permite cumplir con cualquier obligación que tenga de informar sobre discontinuaciones o interrupciones en la fabricación de sus medicamentos, según el Título 21 del Código de los Estados Unidos, artículo 356C(b), y permite a la FDA considerar, lo antes posible, las medidas necesarias, si las hubiera, para evitar la escasez y proteger la salud de los pacientes que dependen de sus productos.
Esta carta le notifica nuestros hallazgos y le brinda la oportunidad de corregir las deficiencias señaladas. Dentro de los 15 días hábiles siguientes a la recepción de esta carta, debe notificar a esta oficina por escrito las medidas que ha tomado para evitar infracciones similares en el futuro. Si no se aborda este asunto adecuadamente, se podrían tomar medidas regulatorias. Si considera que ha cumplido con la Ley FD&C y las regulaciones pertinentes, incluya su razonamiento y cualquier información de respaldo para nuestra consideración.
----------
Más noticias en Urgente24
Aseguradoras complicadas y nuevo caso tras Boston, Escudo, Orbis, Caledonia, La Nueva, Profru....
Escándalo con precios en Mercado Libre: Revelan el secreto que paralizó a todos
Lo que contó Marcos Galperin sobre Mercado Libre que alarma a millones: "Desaparece"
Alpine lanzó la peor noticia para Franco Colapinto: "Difícil"
Finalissima 2026: Filtran en dónde se jugaría Argentina vs España